Wenn die Lymphknoten das Leben bedrohen
Bei Morbus Hodgkin, inzwischen auch sehr oft als „Hodgkin Lymphom“ bezeichnet, handelt es sich um einen Sammelbegriff für verschiedene Arten von Lymphomen. Diese sind in der Regel sehr gut zu behandeln und stellen inzwischen ein weitaus geringeres Risiko dar, als noch vor einigen Jahrzehnten der Fall. Dennoch sollte man sich darüber im Klaren sein, dass es sich bei diesem Leiden um eine Form von Krebs handelt, die man auf keinen auf die leichte Schulter nehmen sollte.
Alles in allem aber ist von einem Behandlungserfolg auszugehen, insbesondere aber dann, wenn die Krankheit bereits früh erkannt wurde. Die genauen Ursachen, die zur Entstehung von Morbus Hodgkin beitragen, sind noch unbekannt.
Steckbrief: Morbus Hodgkin
Inhaltsverzeichnis
- 1 Steckbrief: Morbus Hodgkin
- 2 Definition Hodgkin-Lymphom
- 3 Was ist Morbus Hodgkin?
- 4 Ursachen & Auslöser
- 5 Risikofaktoren
- 6 Symptome & Anzeichen
- 7 Diagnose & Krankheitsverlauf
- 8 Häufigkeit & Statistiken
- 9 Komplikationen & Folgen
- 10 Wann zum Arzt?
- 11 Behandlung & Therapie
- 12 Vorbeugung & Prävention
- 13 Prognose zur Heilung
- 14 Hodgkin Subtypen
- 15 Alternative Medizin
- 16 FAQ – Fragen & Antworten
- Name(n): Morbus Hodgkin; Hodgkin Lymphom
- Art der Krankheit: Krebserkrankung
- Verbreitung: Weltweit
- Erste Erwähnung der Krankheit: 1832
- Behandelbar: Meistens
- Art des Auslösers: Nicht geklärt; vermutlich diverse Viren
- Wieviele Erkrankte: Ca. 0;2% der Weltbevölkerung
- Welchen Facharzt sollte man aufsuchen: Hausarzt; Onkologe
- ICD-10 Code(s): c81.0 – c81.3; c81.7; c81.9
Table of Contents
Definition Hodgkin-Lymphom
Morbus Hodgkin ist eine Art von Lymphom, von dem allgemein angenommen wird, dass es durch Fehlleistungen der weißen Blutkörperchen, den Lymphozyten, ausgelöst wird.
Symptome können unter anderem Fieber, Nachtschweiß und Gewichtsverlust sein. Oft aber stellen sich lediglich nicht schmerzhafte, vergrößerte Lymphknoten im Nacken, unter den Armen oder in der Leistengegend ein. Betroffene leiden oftmals an starkem Juckreiz oder fühlen sich dauerhaft übermüdet.
Etwa die Hälfte aller Fälle von Morbus Hodgkin sind auf eine vorherige Belastung mit dem Epstein Barr Virus zurückzuführen. Weitere Risikofaktoren sind auch eine familiäre Vorbelastung mit der Krankheit sowie hiv / aids.
Es gibt zwei Haupttypen von Hodgkin Lymphomen: Das klassische Hodgkin Lymphom und das noduläre Lymphozyten-prädominante Hodgkin Lymphom. Die Diagnose erfolgt durch Auffinden von Hodgkinzellen.
Morbus Hodgkin kann mit Chemotherapie, Strahlentherapie und Stammzelltransplantation behandelt werden. Die Wahl der Behandlung hängt oft davon ab, wie fortgeschritten der Krebs bereits ist und ob er für eine solche Behandlung günstige Eigenschaften aufweist oder nicht. In frühen Krankheitsstadien ist eine Heilung oftmals noch möglich.
Der Anteil der Menschen, die fünf Jahre nach einer erfolgreichen Behandlung überleben, beträgt in der EU ca. 90%. Für die unter 20 Jährigen beträgt die Überlebensrate sogar allgemein 97%. Strahlentherapie und einige Chemotherapeutika erhöhen jedoch in den folgenden Jahrzehnten das Risiko für die Entstehung anderer Krebsarten, Herzerkrankungen oder Lungenerkrankungen.
Im Jahr 2015 litten etwa 500.000 Menschen an Morbus Hodgkin und 20.000 davon starben starben. In der EU sind in etwa 0,18% der Menschen irgendwann im Laufe ihres Lebens von der vorliegenden Krankheit betroffen.
Das häufigste Diagnosealter liegt zwischen 20 und 40 Jahren. Es wurde nach dem englischen Arzt Thomas Hodgkin benannt, der die Erkrankung erstmals bereits 1832 beschrieb.
Was ist Morbus Hodgkin?
Hodgkin, auch Morbus Hodgkin oder Hodgkin-Lymphom, ist eine bösartige Tumorerkrankung der Lymphknoten.
Wichtigstes Anzeichen sind schmerzlos geschwollene Halslymphknoten. als maligne Lymphome bezeichnet man Krebserkrankungen, die von lymphatischem Gewebe (Lymphknoten, Milz und Rachenmandeln) ausgehen. Dazu gehören neben Hodgkin auch das Non-Hodgkin–Lymphom.
Bei Morbus Hodgkin treten charakteristische Zellveränderungen der B-Lymphozyten auf, die Hodgkin-Zellen und die Reed-Sternberg-Zellen (mehrkernige Riesenzellen). Hodgkin-Erkrankungen machen nur etwa 0,5% aller Krebserkrankungen aus, können aber durch Streuung über den Blutweg in anderen Organen Metastasen bilden.
Die Ursachen sind unbekannt. Möglicherweise kann Hodgkin durch Virusinfektionen wie Epstein-Barr oder hiv ausgelöst werden. Auch erbliche Faktoren können als Ursache in Frage kommen.
Zu den Symptomen gehören schmerzhaft geschwollene Lympknoten, besonders im Halsbereich und unter den Achseln, Leistungsschwäche, Gewichtsverlust, Husten, Juckreiz, Nachtschweiß und Alkoholschmerz (Schmerz in den Lymphknoten nach Alkoholgenuss).
Hodgkin kann sich auf die Milz und über den Blutweg auf weitere Organe wie Leber und Knochen ausbreiten. Daher können als Symptome Splenomegalie, Hepatomegalie, Knochenbrüche und Blutbildveränderungen durch Knochenmarksinfiltration auftreten.
Durch Lymphknotenbiopsie und histologische Untersuchung der Gewebeprobe können die Hodgkin-Zellen und Reed-Sternberg-Zellen nachgewiesen und Morbus Hodgkin eindeutig diagnostiziert werden.
Bei der Diagnose von Hodgkin unterscheidet man vier Schweregrade der Erkrankung. Bei Stadium I ist nur ein Lymphknoten befallen, bei Stadium IV hat sich die Krebserkrankung bereits auf andere Organe ausgebreitet.
Durch Abtasten von Lymphknoten, Milz und Leber kann der Arzt die Organgröße bestimmen. Durch Röntgen, CT (Computertomografie) und MRT (Magnetresonanztomografie) können die Krankheitsherde bildlich dargestellt werden. Zusätzlich werden in Blutuntersuchungen die Nieren– und Leberwerte bestimmt.
Therapie Ziele
Hodgkin wird vor allem durch eine Kombination von Chemotherapie und Strahlentherapie behandelt. Wegen der dabei möglichen Nebenwirkungen sollte vor Therapiebeginn die Funktion wichtiger Organe untersucht werden.
Die Therapie zielt darauf ab, das erkrankte Gewebe zu zerstören. Tumorzellen sind anfälliger als gesunde Zellen und werden daher bei Bestrahlung mit Röntgenstrahlen als erste abgetötet. Die Chemotherapie erfolgt mit einer Kombination verschiedener Zytostatika, die in regelmäßigen Abständen, sogenannten Zyklen, verabreicht werden.
Nach den Anfangsbuchstaben der dabei eingesetzten Zytostatika wird das Behandlungsschema als BEACOPP bezeichnet. Zur Behandlung gehört auch eine Anpassung der Chemotherapiezyklen an laufend durchgeführte Kontrolluntersuchungen der Blutwerte.
Bei Unterschreiten bestimmter Grenzwerte an Blutzellen kann die Dosis verringert oder die Abstände der Chemotherapiezyklen verlängert werden. Hodgkin kann auch durch eine Knochenmarkstransplantation oder eine Stammzellentransplantation behandelt werden.
Für viele Hodgkin-Kranke ist der Erfahrungs- und Informationsaustausch in einem Forum ein stabilisierender Faktor. Die Anthroposophische Medizin setzt bei Krebserkrankungen Mistelpräparate ein. Ergänzend zur schulmedizinischen Therapie können auch die homöopathischen Mittel Barium carbonicum, Barium jodatum sowie Kalium carbonicum und Kalium jodatum eingesetzt werden.
Vor Auswahl eines homöopathischen Mittels sollte man die Mittelbeschreibungen genau lesen und dasjenige Mittel wählen, das am besten zur eigenen Situation passt. Barium carbonicum sollte mehrere Monate eingenommen werden, da die Wirkung hier langsam einsetzt. Laut den Mittelbeschreibungen sind Barium carbonicum und Barium jodatum für Menschen geeignet, die schüchtern und scheu wirken.
Kalium jodatum ist geeignet, wenn Schwitzen als Begleitsymptom auftritt. Die Mittel sind in D3 bis D12 zu verwenden. Zusätzlich werden bei Krebserkrankungen hohe Dosen Vitamin C empfohlen.
Ursachen & Auslöser
Bis heute konnte trotz intensiver Forschung noch nicht zufriedenstellend geklärt werden, welche Ursachen dazu führen, dass es zu einer Entstehung von Morbus Hodgkin kommt. Nichtsdestoweniger aber konnten einige Mechanismen erkannt werden, die einer Erkrankung mit Morbus Hodgkin direkt voraus gehen. Diese ist im Falle der vorliegenden Erkrankung eine genetische Mutation der Lymphocyten.
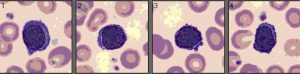
Lymphozyten
Ein Lymphozyt ist eine der Unterformen der weißen Blutkörperchen im Immunsystem eines Wirbeltieres. Lymphozyten umfassen die sog. natürlichen Killerzellen (die in zellvermittelter, cytotoxischer angeborener Immunität wirken), T-Zellen (für zellvermittelte, zytotoxische adaptive Immunität) und B-Zellen (für humorale, antikörpergesteuerte adaptive Immunität). Sie sind die wichtigste Art von Zellen in den Lymphen, daher auch der Name „Lymphozyten“.
Im Falle einer Erkrankung mit Hodgkin, veranlasst der Körper diese Zellen dazu, sich rapide zu vermehren, was wiederum das Entstehen von Hodgkin einleitet. Im Laufe der Zeit sorgt diese krankhafte Vermehrung der genetisch veränderten Zellen darüber hinaus dafür, dass sie die genetisch unveränderten, sprich die gesunden Zellen, früher oder später überwältigen.
Ist dieser Fall eingetreten, so können sich die krankhaften Zellen regelrecht ungehindert „austoben“. Zudem verformen sich die erkrankten Zellen immer mehr, sodass sie schließlich auch abnormal groß sind, was die daraus entstehenden Symptome noch mehr verstärkt.
Auch sollte man an dieser Stelle nicht vergessen, dass es mehrere Arten von Morbus Hodgkin gibt, die nur allgemein unter dem Sammelbegriff Hodgkin Lymphom zusammengefasst werden. Je nachdem welche Art von Morbus Hodgkin vorliegt, ist ausschlaggebend dafür, welche Symptome sich einstellen und welche Behandlungsmethoden notwendig sind, um eine Heilung zu gewährleisten.
Risikofaktoren
Wie bereits eingänglich erwähnt, lassen sich zwar keine genauen Ursachen feststellen, dennoch aber gibt es einige Risikofaktoren, die immer wieder mit Morbus Hodgkin in Verbindung gebracht werden, Leider allerdings handelt es sich hierbei nicht immer um grundsätzlich vermeidbare Risikofaktoren, sodass man manchmal schlicht damit leben muss, einer Risikogruppe anzugehören.
Mögliche Risikofakten von Morbus Hodgkin sind:
- Alter
- Familiäre Vorbelastung
- Geschlecht
- Epstein-Barr Virus
Diese werden nachfolgend noch genauer erläutert.
Abschließend bleibt also zu bemerken, dass Personen, die Teil einer oder gar mehrerer Risikogruppen sind, ein besonderes Augenmerk auf etwaige Symptome haben sollten und darüber hinaus auch nicht davor zurückscheuen sollten, einen Arzt aufzusuchen, wenn sie fürchten, dass sie betroffen sein könnten. Wird die Krankheit früh erkannt, ist es sehr viel leichter möglich, diesem Leiden Herr zu werden.
Alter
Das Voranschreiten des Alters spielt bei sehr vielen Erkrankungen eine maßgebliche Rolle und nicht selten gilt die Faustregel, dass je älter man ist, desto anfälliger ist man für viele Leiden und Gebrechen. Dasselbe gilt leider auch für Morbus Hodgkin.

Mit fortschreitendem Alter steigt auch das Hodgkin-Risiko
Dennoch verhält es sich bei der vorliegenden Erkrankung etwas merkwürdig. Das Alter und die Wahrscheinlichkeit an an einem solchem Lymphom zu erkranken, greifen nicht gradlinig ineinander, will meinen, dass ein höheres Alter nicht auch immer automatisch bedeutet, dass man stärker gefährdet ist.
Am häufigsten tritt Morbus Hodgkin nämlich zwischen dem 15 und den 30 Lebensjahr auf, dann aber statistisch erst wieder besonders häufig nach dem 55. Lebensjahr. Das heißt kurzum, dass die Menschen zwischen ihrem 30. und 55. Lebensjahr oftmals nicht Opfer dieses Leidens werden.
Dennoch natürlich muss dies nicht heißen, dass man gleichsam immun gegen die Erkrankung ist. Auftreten kann sie immer. Nicht zuletzt darum ist es absolut notwendig, bei einem Arzt vorstellig zu werden, wenn man fürchtet, dass man an der vorliegenden Erkrankung leiden könnte. Frühe Hilfe ist hier das A und O.
Familiäre Vorbelastung
Kommt es innerhalb einer Familie häufiger zu Fällen von Krebs oder anderen ähnlichen Leiden, wie beispielsweise dem Morbus Hodgkin, so sollte man dies zum Anlass nehmen, besondere Vorsicht walten zu lassen und sich in regelmäßigen Abständen untersuchen zu lassen, auch wenn dafür symptomatisch zunächst keine Veranlassung besteht.
Denn oftmals konnte beobachten werden, dass gerade Morbus Hodgkin eine Tendenz zeigt, eine regelrechte Familienkrankheit zu sein.
Sicherlich ist nicht jeder automatisch auch betroffen, der einen Elternteil oder ein Geschwister mit dieser Krankheit hat, aber dennoch sollte man vorsichtig sein und bereits kleinste Alarmzeichen zum Anlass nehmen, sich untersuchen und testen zu lassen.
Denn allein statistisch gesehen, ist die Wahrscheinlichkeit, dass man, so man einer Familie angehört, in der diese Krankheit besonders häufig auftritt, auch selbst stärker gefährdet ist, als andere Personen ohne eine familiäre Vorbelastung.
Kurzum also sollte man sich, insofern in der näheren Verwandtschaft bereits Fälle von Morbus Hodgkin festgestellt werden konnten, auch jeden Fall vertrauensvoll einem Arzt zuwenden und sich vorsichtshalber testen lassen.
Geschlecht

Männer sind häufiger betroffen
Pixabay / geralt
Gleich zu Beginn sei gesagt, dass es beide Geschlechter treffen kann. Dennoch trifft es Vertreter des männlichen Geschlechts statistisch gesehen häufiger als weibliche Personen. Die Unterschiede sind allerdings nicht allzu groß.
Nichtsdestotrotz sollte man sich darum, gerade wenn man selbst männlich ist, darüber hinaus noch im „richtigen“ Alter und familiär vorbelastet ist, nicht bitten lassen und in regelmäßigen Abständen die Möglichkeit wahrnehmen, sich auf Morbus Hodgkin hin testen zu lassen.
Vorsicht ist besser als Nachsicht. Dieses Faktum kann man in der modernen Schulmedizin gar nicht überbetonen. Zu viele Patienten suchen erst dann einen Arzt auf, wenn es bereits zu spät ist.
Epstein-Barr Virus
Menschen, die Krankheiten hatten, die durch das Epstein Barr Virus ausgelöst wurden, weisen in aller Regel ein höheres Risiko auf, an einer Form von Morbus Hodgkin zu erkranken.Epstein-Barr ist das Virus, das unter anderem Mononukleose verursacht.
Vielleicht ist diese Krankheit besser unter den Namen „Mono“ oder „Pfeiffersches Drüsenfieber“ bekannt. Sie wird auch die „Kuss Krankheit“ genannt, da eine Ansteckung mittels Küssen ein sehr verbreiteter Weg der Übertragung ist. Obwohl das Epstein-Barr-Virus (EBV) kein allzu in der Öffentlichkeit bekannter Name ist, sind viele Menschen mit diesem Virus infiziert, ohne es jedoch zu wissen. Viele Menschen tragen das Virus ruhend in sich, er bricht aber nicht aus und sie werden auch nicht krank.
Sobald man sich mit EBV infiziert hat, können sich Symptome einstellen und 4 bis 6 Wochen dauern. Alles in allem jedoch sind die zu erwartenden Symptome oftmals eher mild. Besonders aber dann, wenn die infizierte Person noch sehr jung ist. Betroffene Kinder beispielsweise weisen trotz einer ausgebrochenen Krankheit nur selten nennenswerte Symptome auf.
Anzeichen
Insofern überhaupt Symptome auftreten, erinnern diese mehr an eine Grippe als an alles andere. Jugendliche dagegen, bei denen die Krankheit auftritt, sind oftmals sehr viel stärker betroffen und es kommt zu nicht unwesentlichen Erscheinungen der Krankheit.
Hierunter zählen unter anderem:
- Extreme Müdigkeit,
- Fieber,
- Verlust des Appetits,
- Ausschläge aller Arten,
- Entzündungen des Halses und der Kehle,
- geschwollene Drüsen, insbesondere unter den Ohren, Schwäche und Muskelschmerzen.
Auch sollte man nicht vergessen, dass das Pfeiffersche Drüsenfieber mitunter sehr lange anhalten kann und der betroffene Jugendliche für die Dauer der Erkrankung vom Schulbetrieb usw. ferngehalten werden muss.
Zwar sind die gröbsten Symptome meist schon nach zwei bis Vier Wochen vorüber, aber andere Auswirkungen dieses Leidens können durchaus bis zu zu einem halben Jahr anhalten. Insbesondere die eben erwähnte sehr starke Müdigkeit.
Sollte ein Jugendlicher immer sehr Müde sein, könnte also auch eine Erkrankung mit dem Epstein-Barr Virus dahinterstecken.Es gibt sehr viele Wege, über die man sich mit dem Epstein-Barr Virus anstecken kann.
Darunter das bereits erwähnte Küssen ebenso wie ungeschützer Geschlechtsverkehr, der Austausch von Blut, Speichel, Urin, Kot oder anderen Körperflüssigkeiten. Auch beispielsweise die Benutzung einer Zahnbürste einer betroffenen Person kann zu einer Ansteckung führen.
Dessen sollte man sich immer bewusst sein. Nicht zuletzt deswegen sind hier, gerade dann, wenn man um die Ansteckung einer anderen Person weiß, besondere Vorsichtsmaßnahmen zu treffen.
Alles in allem aber sollte man nicht dem Irrglauben verfallen, dass man, nur weil man mit dem Epstein-Barr Virus infiziert ist, auch früher oder später an Morbus Hodgkin leiden wird. Zwar ist die Wahrscheinlichkeit dafür sicherlich höher, aber ein Garant ist es glücklicherweise nicht.
Symptome & Anzeichen
Zunächst einmal sei gesagt, dass der Morbus Hodgkin nicht immer mit besonders gravierenden Symptomen einhergehen muss. Bisweilen bemerkt die betroffene Person lange Zeit nicht, dass etwas nicht stimmt und lässt sich darum nicht untersuchen, das führt mittelfristig zu einigen Problemen, besonders eine zu spät einsetzende Behandlung birgt sehr viele Risiken, die nicht unterschätzt werden sollten.
Schließlich und endlich handelt es sich bei dem vorliegenden Leiden um eine Form von Krebs und mit Krankheiten dieser Art ist bekanntlich niemals zu Spaßen. Nicht zuletzt darum ist es absolut notwendig, die etwaig auftretenden Symptome nicht auf die leichte Schulter zu nehmen und sich bereits bei kleinen Verdachtsmomenten adäquate Hilfe zu suchen.

Pixabay / nastya_gepp
Hierzu eine Übersicht der gängigsten Symptome:
- Anschwellen der Lymphknoten
- Fieberschübe
- Nächtliches Schwitzen
- Gesteigerte Anfälligkeit gegenüber Alkohol
- Unfreiwilliger Gewichtsverlust
- Starkes Hautjucken
- Dauerhafte Müdigkeit
Lymphknoten-Schwellung
Anschwellen der Lymphknoten
:
Morbus Hodgkin wird oftmals auch als Lymphom bezeichnet. Es ist also kein besonderes Kunststück, den Zusammenhang zwischen dieser Erkrankung und einer krankhaften Veränderungen der Lymphknoten zu erkennen. Oftmals schwellen besonders die Lymphknoten in den Achselhöhlen, im Hals und im Bereich der Leiste an.
Ein solches Anschwellen jedoch kann sehr viele Gründe haben und muss nicht immer ein Zeichen dafür sein, dass man Opfer des Morbus Hodgkin ist. Tatsächlich sind die Gründe hierfür zumeist eher harmlos. Denn auch schon bei einer leichten Grippe schwellen diese Lymphknoten an.
Für den Laien kann es darum bisweilen schwer sein zu evaluieren, welche Gründe dem Anschwellen zugrunde liegen. Das Bedeutet im Umkehrschluss, dass es immer ratsam ist, ärztlichen Rat einzuholen. Insbesondere aber dann, wenn einem das Anschwellen der Lymphknoten besonders seltsam oder atypisch vorkommt.
Andauernde Müdigkeit
Dauerhafte Müdigkeit
Chronische Müdigkeit und Erschöpfung sind Phänomene, mit denen die Menschen in der modernen Leistungsgesellschaft sehr häufig zu kämpfen haben. Darum nehmen viele diesen Zustand schon gar nicht mehr als besonders bedrohlich wahr, sondern haben gelernt, irgendwie damit zu leben.
Das ist nicht nur sehr gefährlich, sondern trübt einem auch den Blick darauf, was eventuell mit einem nicht stimmen könnten. Denn sehr viele Krankheiten äußern sich gerade in ihren Anfängen in einer chronischen Erschöpfung. So auch in vielen Fällen der Morbus Hodgkin.
Wer also unter einer andauernden Müdigkeit, die darüber hinaus auch noch mit einer sehr starken Erschöpfung und Antriebslosigkeit einhergeht leidet, der sollte so schnell als möglich darob einen Arzt konsultieren.
Die Gründe hierfür können banal sein, manchmal aber steckt doch mehr dahinter.Auch ist es nicht immer leicht festzustellen, ob Müdigkeit und Erschöpfung nun aufgrund einer Krankheit entstehen oder eventuell aufgrund einer Überforderung im Beruf oder im Alltag. Auch darum ist es wichtig, dieses Symptom nicht leichtfertig abzutun.
Juckreiz & Gewichtsverlust
Starkes Hautjucken
Plötzliches und vorallem auch sehr starkes Hautjucken, dem keine erkennbaren Auslöser zugrunde liegen, sollte einem ebenso als Warnsignal dafür gelten, dass etwas mit einem nicht stimmt. Oftmals handelt es sich hierbei um Erkrankungen der Haut selbst, aber auch einige Arten von Hodgkin äußern sich mit diesem Symptom.Sollte man also zuvor niemals Probleme mit Hautjucken gehabt haben und diesem Phänomen zum ersten Mal in dieser Stärke begegnen, so sollte man den Gang zum Arzt nicht scheuen.
Unfreiwilliger Gewichtsverlust
Nicht selten kommt es vor, dass man, bevor die Krankheit als solche überhaupt erst festgestellt wird, unfreiwillig einiges an Gewicht verliert. Dies geschieht komplett ohne das Zutun des Individuums, sprich keine besonderen Diäten oder Sport.
Hierbei kann der Gewichtsverlust mitunter sehr rapid und gravierend sein. Wer also derartige Symptome an sich oder anderen beobachtet, sollte diese auf jeden Fall als Warnsignal verstehen und entsprechend tätig werden.
Alkohol-Unverträglichkeit
Gesteigerte Anfälligkeit gegenüber Alkohol
Wer plötzlich keinen Alkohol mehr verträgt oder aber nur noch geringste Mengen davon, der könnte eventuell Opfer eines Lymphoms, sprich des Morbus Hodgkin sein. Zwar gibt es auch hierfür diverse andere Gründe, nicht selten aber steht die vorliegende Krankheit damit in direktem Zusammenhang.
Auch kann es durchaus sein, dass die Lymphknoten also solche beginnen zu schmerzen, wenn man Alkohol konsumiert. Diesen Umstand, so er denn Eintritt, sollte einem als absolutes Warnsignal gelten, dem sofort nachzugehen ist.
Schwitzen & Fieber
Nächtliches Schwitzen
Auch wer beginnt, nachts plötzlich stark zu schwitzen, ohne jemals zuvor solche Probleme gehabt zu haben, sollte dies als Warnsignal dafür nehmen, dass etwas mit dem Lymphknoten nicht in Ordnung sein könnten.Es ist also ratsam, diesen Umstand bei der nächsten Routineuntersuchung zu erwähnen.
Fieberschübe
Personen, die an Morbus Hodgkin leiden, neigen zu immer wieder scheins grundlos auftretenden Fieberschüben. Sollte das ein Problem sein, mit dem man selbst auch zu kämpfen hat, sollte man sich deswegen sofort zu einem Arzt begeben. Zwar muss es nicht Morbus Hodgkin sein, aber auf die leichte Schulter nehmen, sollte man Fieber niemals.
Diagnose & Krankheitsverlauf
Morbus Hodgkin muss von nicht-kanzerösen Ursachen der Lymphknotenschwellung (wie verschiedene Infektionen) und von anderen Krebsarten unterschieden werden. Eine definitive Diagnose ist durch eine Lymphknotenbiopsie (in der Regel eine Exzisionsbiopsie mit mikroskopischer Untersuchung) möglich.
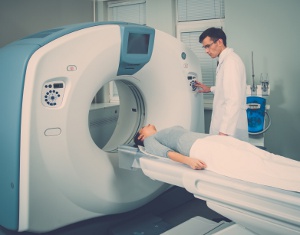
Eine Computertomographie (CT)
Bluttests werden auch durchgeführt, um die Funktion der wichtigsten Organe zu beurteilen und die Sicherheit für eine etwaige Chemotherapie vor Beginn der Behandlung zu bewerten.
Die sogenannte Positronen-Emissions-Tomographie (PET) wird verwendet, um kleine Ablagerungen zu erkennen, die beim CT-Scan nicht sichtbar gemacht werden können. PET-Scans sind darüber hinaus auch nützlich für die funktionelle Bildgebung (durch Verwendung einer radioaktiv markierten Glucose, um Gewebe mit erhöhtem Metabolismus abzubilden). In einigen Fällen muss ein Gallium-Scan anstelle eines PET-Scan verwendet werden.
Im Folgenden ein Überblick über die gängigsten Diagnoseverfahren:
Untersuchung
Allgemeine körperliche Untersuchung
Bei einer solche Untersuchung prüft der behandelnde Arzt, ob die Lymphknoten des Patienten geschwollen sind. Insbesondere jene im Bereich des Halses, der Unterarme und der Leiste, aber auch Verhärtungen und Schwellungen im Bereich der Leber und der Nieren können und sollten vom zuständigen Arzt abgetastet werden.
Eine solche Untersuchung jedoch ersetzt auf keinen Fall medizinische Tests und dient nur einer allerersten Evaluierung der medizinischen Situation des Patienten. Man kommt also auf keinen Fall darum herum, sich weiteren Tests zu unterziehen, wenn man Gewissheit, über seine Situation haben möchte. Der behandelnde Arzt wird einen nach der ersten allgemeinen Untersuchung beraten, welche Schritte als nächstes zu unternehmen sind.
Bluttest
Bei einem handelt es sich Bluttest um eine Laboranalyse, die an einer Blutprobe durchgeführt wird, die normalerweise aus einer Armvene mit einer hypodermischen Nadel oder über einen Stich in die Fingerkuppe entnommen wird. Mehrere Tests für spezifische Blutbestandteile, wie z. B. ein Glukosetest oder ein Cholesterintest, werden oft zu einem Testpanel zusammengefaßt, das als kleines oder großes Blutbild bezeichnet wird.
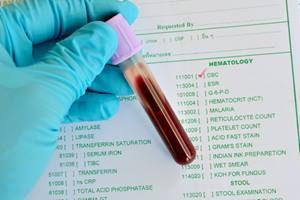 Bluttests werden häufig im Gesundheitswesen verwendet, um physiologische und biochemische Zustände, wie Krankheit, Mineralgehalt, Arzneimittelwirksamkeit und Organfunktion zu bestimmen. Bluttests werden auch als Drogentests verwendet, um Drogenmissbrauch zu erkennen.
Bluttests werden häufig im Gesundheitswesen verwendet, um physiologische und biochemische Zustände, wie Krankheit, Mineralgehalt, Arzneimittelwirksamkeit und Organfunktion zu bestimmen. Bluttests werden auch als Drogentests verwendet, um Drogenmissbrauch zu erkennen.
Die Blutabnahme ist nützlich, da es sich um eine minimal-invasive Methode handelt, um Zellen und extrazelluläre Flüssigkeit aus dem Körper für die Analyse zu gewinnen. Blut fließt durch den Körper und dient als Medium, um das Gewebe mit Sauerstoff und Nährstoffen zu versorgen und darüber hinaus Abfallprodukte zur Entsorgung in die Ausscheidungssysteme zurückführt.
Folglich beeinflusst der Zustand des Blutes den allgemeinen physisches Zustand. Aus diesen Gründen sind Bluttests die am häufigsten durchgeführten medizinischen Tests. Wenn nur ein paar Tropfen Blut benötigt werden, wird ein sogenannter „Fingertipp“ durchgeführt. Hierbei wird lediglich die Fingerkuppe mit einer Nadel angestochen. Das Abpumpen größerer Mengen Blut aus der Armvene kann somit vermieden werden.
Zumeist sind Krankenschwestern und Ärztehelfer diejenigen, die mit der Blutentnahme von Patienten beauftragt werden. Unter bestimmten Umständen ist es jedoch manchmal Ärztesache, das Blut eines Patienten zu entnehmen. Die aus einer solchen Analyse gewonnen Daten können zwar nicht zu 100% klären, ob Morbus Hodgkin vorliegt, aber die Wahrscheinlichkeit dafür lässt sich besser darstellen.
Bildgebende Verfahren
Unter der medizinischen Bildgebung versteht man die Technik, die zur Sichtbarmachung des Inneren eines Körpers zwecks klinischer Analysen und medizinischer Eingriffe dient, sowie die visuelle Darstellung der Funktion einiger Organe oder Gewebes (Physiologie).
Die medizinische Bildgebung soll innere Strukturen aufdecken, die normalerweise von Haut und Knochen verdeckt werden, sowie dabei helfen, Krankheiten zu diagnostizieren und / oder zu behandeln. Bildgebende Verfahren dienen manchmal auch dazu, Vergleichswerte zu gewinnen, um gesundes Gewebe besser von krankem unterscheiden zu können.
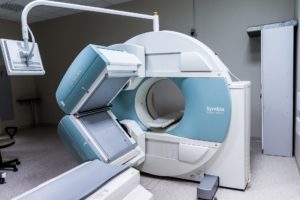
Magnetresonanztomograph (MRT)
Die Disziplin, die sich mit der medizinischen Bildgebung auseinandersetzt, bezeichnet man als Radiologie. Magnetresonanztomographie, medizinischer Ultraschall, Endoskopie, Elastographie, taktile Bildgebung, Thermografie, medizinische Fotografie und nuklearmedizinische funktionelle bildgebende Verfahren wie Positronen-Emissions-Tomographie (PET) und Single-Photon-Emissions-Computertomographie (SPECT) gehören zu den gängigsten verfahren.
Bei Morbus Hodgkin, kommen insbesondere PETs zum Einsatz. Mess- und Aufzeichnungstechniken, die nicht primär zur Erzeugung von Bildern gedacht sind, wie:
- Elektroenzephalographie (EEG)
- Magnetoenzephalographie (MEG)
- Elektrokardiographie (EKG)
- und andere
stellen andere Technologien dar, die eher den zeitlichen Effekt gewisser Tätigkeiten auf den Organismus darstellen.
Von Laien werden diese bisweilen verwechselt oder falsch zugeorndet.Die medizinische Bildgebung wird oft als eine Technik angesehen, die nichtinvasiv Bilder des Inneren des Körpers erzeugen kann.
Dies bedeutet, dass der behandelnde Arzt dazu in der Lage ist, die Erkrankungen des Patienten zu erkennen, ohne diesen dafür aufschneiden zu müssen, wie es lange Zeit vorher der Fall war. Gerade bei Morbus Hodgkin und anderen ähnlichen Erkrankungen sind bildgebende Verfahren in der Diagnose sehr wichtig.
Knochemarksanalyse
Unter einer sogenannten Knochenmarkbiopsie oder Knochenmarkaspiration versteht man Verfahren, die zum Sammeln und Untersuchen von Knochenmark, das schwammartige Gewebe in einigen Ihrer größeren Knochen, angewendet werden.
Knochenmarkbiopsie und Aspiration können zeigen, ob das Knochenmark gesund ist und normale Blutzellen produziert. Ärzte verwenden diese Verfahren zwecks einer Diagnose und Überwachung von Blutkrankheiten und Knochenmarkerkrankungen, einschließlich einiger Krebserkrankungen, wie beispielsweise auch das vorliegende Hodgkin Lymphom.Knochenmark hat einen flüssigen Teil und einen festeren Teil.
Bei einer Knochenmarkbiopsie führt der Arzt eine Nadel zum Herausziehen einer Probe des festen Anteils ein. Bei der Knochenmarkaspiration wird eine Nadel verwendet, um eine Probe des Fluidanteils herauszuziehen. Knochenmarksbiopsie und Knochenmarkaspiration werden oft gleichzeitig durchgeführt. Zusammen können diese Verfahren Knochenmarkuntersuchung genannt werden.
Lymphknoten entfernen
Manchmal kann es aus medizinischer Sicht empfehlenswert sein, wenn der Arzt den etwaig betroffenen Lymphknoten vollständig oder zumindest teilweise entfernt und mithilfe des somit gewonnenen Gewebes eine Biopsie durchführt.
Eine solche ist in der Regel sehr akkurat und zeigt dem behandelnden Arzt oftmals ohne Widersprüchlichkeiten an, ob Morbus Hodgkin vorliegt oder nicht. Allerdings ist diese Methode nicht immer empfehlenswert. Es kommt hier sehr stark auf den individuellen Fall und den Patienten an. Darüber hinaus birgt die Entnahme eines Lymphknoten auch einige Risiken, die vor der Prozedur abzuwägen sind.
Zusammenfassung
Darüber hinaus ist es oftmals notwendig, verschiedene Diagnoseverfahren anzuwenden, um komplett auf Nummer sicher gehen zu können. So kommen neben den üblichen bildgebenden Verfahren auch beinahe immer Biopsien und dergleichen in Anwendung.
Es ist kaum möglich, eine Diagnose alleine auf die Ergebnisse eines einzelnen medizinischen Tests aufzubauen. Darum muss man sich als potentiell betroffenes Individuum darauf einstellen, mehrere Testverfahren über sich ergehen lassen zu müssen. Allerdings brauchen diese oftmals keine allzu lange Zeit und sind mehr oder weniger schmerzlos.
4 Hodgkin Stadien
Die verschiedenen Stadien von Morbus Hodgkin
Die moderne Schulmedizin unterscheidet vier Stadien des Morbus Hodgkin:
- 1. Stadium: Der Krebs ist auf einen einzelnen Lymphknoten oder ein einzelnes Organ beschränkt, hat also noch keine weiteren Teile des Organismus befallen.In diesem Stadium lässt sich der Morbus Hodgkin zumeist noch sehr gut behandeln.
- 2. Stadium: In diesem Stadium befindet sich der Krebs bereits in zwei Lymphknotenregionen oder aber der Krebs ist in ein Organ und die nahe gelegenen Lymphknoten eingedrungen. Aber der Krebs ist immer noch auf einen definierbaren Teil des Körpers beschränkt, entweder oberhalb oder unterhalb des Zwerchfells.Auch in diesem Stadium lässt sich das leiden noch vergleichsweise gut behandeln.
- 3. Stadium: Wenn sich der Krebs zu Lymphknoten sowohl oberhalb als auch unterhalb des Zwerchfells bewegt, so spricht man vom dritten Stadium. Der Krebs kann auch in einem Teil des Gewebes oder eines Organs in der Nähe der Lymphknotengruppen oder in die Milz eingedrungen sein.Eine Behandlung in diesem Stadium fällt oftmals wesentlich schwerer und ist nicht immer erfolgreich. Die Chancen auf Heilung jedoch sind auch hier sehr individuell und müssen von Fall zu Fall neu evaluiert werden.
- 4. Stadium: Dies ist das am weitesten fortgeschrittene Stadium des Hodgkin Lymphoms. Die Krebszellen befinden sich bereits in mehreren Teilen eines oder mehrerer Organe und Gewebe. Das vierte Stadium des Hodgkin Lymphoms betrifft nicht nur die Lymphknoten, sondern auch andere Teile des Körpers, wie die Leber, Lunge oder Knochen.Eine Heilung in diesem Stadium ist zwar nicht ausgeschlossen, dennoch stehen die Chancen alles in allem eher schlecht. Nicht zuletzt deswegen ist es, wie bereits schon mehrfach erwähnt, absolut notwendig, sich rechtzeitig testen, untersuchen und behandeln zu lassen.
Häufigkeit & Statistiken
Das Hodgkin Lymphom gehört nicht zu den 20 häufigsten Krebserkrankungen Deutschland und Europa, macht aber dennoch nur weniger als 1% aller neuen Krebsfälle aus. Bei Männern in Europa ist Morbus Hodgkin die 19. häufigste Krebserkrankung (weniger als 1% aller neuen männlichen Krebsfälle). Bei Frauen im europäischen Raum gehört das Leiden nicht zu den 20 häufigsten Krebserkrankungen (weniger als 1% aller neuen Krebsfälle bei Frauen).
Die Inzidenz für Morbus Hodgkin zeigt eine klare bimodale Altersverteilung, wobei der erste Höhepunkt bei den Inzidenzraten bei jungen Erwachsenen und der zweite bei älteren Männern und Frauen lag, wobei die höchsten Inzidenzraten jedoch bei älteren Menschen lagen.
Alter & Tendenz
In Europa traten in den Jahren 2013 bis 2015 im Durchschnitt jedes Jahr fast 3 von 20 (13%) der neuen Fälle bei Menschen im Alter von 75 Jahren und älter auf. Die altersspezifischen Inzidenzraten steigen in der Kindheit stark an und liegen bei jungen Erwachsenen zwischen 20 und 24 Jahren am höchsten.
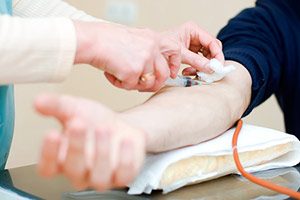 Die Raten sinken dann bis zum mittleren Alter wieder ab, bevor sie wieder erneut ansteigen, um schließlich einen zweiten Höhepunkt zu erreichen. Die höchsten Raten liegen in der Altersgruppe der 75 bis 79 Jährigen Männer und der Altersgruppe der 20 bis 24 Jährigen Frauen.
Die Raten sinken dann bis zum mittleren Alter wieder ab, bevor sie wieder erneut ansteigen, um schließlich einen zweiten Höhepunkt zu erreichen. Die höchsten Raten liegen in der Altersgruppe der 75 bis 79 Jährigen Männer und der Altersgruppe der 20 bis 24 Jährigen Frauen.
Die Inzidenzraten sind bei Männern in einer Reihe von (hauptsächlich älteren) Altersgruppen signifikant höher als bei Frauen. Der Abstand ist im Alter von 0 bis 4 Jahren am größten, wenn die altersspezifische Inzidenzrate bei Männern 6 bis 7 mal höher ist als bei Frauen.
Bei Männern nahmen die Fälle von Morbus Hodgkin im europäischen Vergleich zwischen 1993 und 1995 sowie zwischen 2013 und 2015 um 32% zu. Bei Frauen nahmen die Inzidenzraten im europäischen Vergleich sogar zwischen 1993 und 1995 sowie 2013 und 2015 um 40% zu.
Die krankheitsspezifischen Inzidenzraten sind in allen Altersgruppen seit Beginn der 1990er Jahre in europäischen Vergleich gestiegen. Die Raten bei Menschen im Alter von:
- 0 bis 24 Jahren haben um 21% zugenommen,
- 25 bis 49 Jahren um 17% ,
- 50 bis 59 Jahren um 21%,
- 60 bis 69 Jahren um 45%,
- 70 bis 79 Jahren um 108%
- jenseits der 80 um 134%.
Diese Zahlen sind alarmierend. Beim Hodgkin Lymphom spiegeln sich, wie bei den meisten Krebsarten, die Inzidenztrends weitgehend durch die zunehmende Prävalenz von Risikofaktoren und Verbesserungen bei Diagnose und Datenaufzeichnung wider. Die jüngsten Inzidenztrends wurden von der Risikofaktorprävalenz der vergangenen Jahre beeinflusst.
Stadium & Schweregrad
Daten für das Stadium, in dem die Krankheit zumeist diagnostiziert wird, sind für die EU und Deutschland noch nicht verfügbar. Dies lässt sich auf Inkonsistenzen beim Sammeln und Aufzeichnen der sogenannten „Staging-Daten“ in der Vergangenheit zurückführen.
Dies verbessert sich jedoch zusehends und Pläne für einen national konsistenten Datensatz in Deutschland sind bereits angelaufen. Zwischenzeitlich stehen für grobe Einschätzungen der Inzidenz jedoch einige lokale Statistiken zur Verfügung.
Sie decken rund 5% der Bevölkerung der EU ab und sind aber aufgrund von Unterschieden bei den zugrunde liegenden demografischen Faktoren (wie Alter, Vorerkrankungen oder ethnische Zugehörigkeit) sowie unterschiedlichen lokalen Standards und Richtlinien für die Gesundheitsversorgung möglicherweise nicht repräsentativ für das Land insgesamt.
Diagnosedaten
Die Diagnosedaten können, wie bereits erwähnt, bisweilen etwas irreführend sein, besonders aber diejenigen, die aus einer reinen Anamnese gewonnen werden. Müsste man sich alleine auf diese Daten verlassen, so wäre es sehr sehr schwer, Morbus Hodgkin zufriedenstellen festzustellen.
Die auftretenden Symptome sind nämlich alles in allem eher unspezifisch und lassen sich darum neben der vorliegenden Erkrankung auch vielen anderen Erkrankungen zuordnen. Selbst die Kombination für die Krankheit typischer Symptome sind nicht immer einzigartig und können den Blick auf das tatsächlich zugrunde liegende Problem verzerren.
Nicht zuletzt darum ist es absolut notwendig, neben einer klassischen Anamnese, auch noch weitere medizinische Tests durchzuführen. Schließlich und endlich ist Morbus Hodkin nicht immer ganz so leicht zu erkennen. Zumeist bringt erst die Biopsie eines etwaig betroffenen Lymphknotens endgültige Gewissheit darüber, ob es sich aufgrund der vorliegenden Symptome auf ein Vorhandensein eines Lymphoms schließen lassen kann.
Darum sollte man an dieser Stelle lediglich der Schulmedizin vertrauen und für eine Diagnose keine Homöopathen heranziehen. Dieser können bei der Behandlung zwar sicherlich helfen, aber bei der Stellung einer Diagnose dürften sie nicht besonders hilfreich sein.
Alles in allem aber ist es heutzutage, dank der modernen Schulmedizin, kein allzu schwerwiegendes Problem mehr, den Morbus Hodgkin als solchen zu erkennen. Gleichwohl die hierfür angewandten Mittel bisweilen etwas aufwendiger sind, als beispielsweise bei anderen Formen von Krebs.
Somit lässt sich also zusammenfassend erwähnen, dass man sich nicht sorgen muss, eventuell zu die falsche Diagnose gestellt zu bekommen, dennoch aber kann es sein, dass das Prozedere der medizinisches Tests etwas mehr Zeit in Anspruch nimmt, als dies bei anderen Krankheiten der Fall ist.
Nicht zuletzt deswegen ist es besonders empfehlenswert, bereits sehr früh bei einem Arzt vorstellig zu werden und den Gang zum Doktor nicht bis auf die letzte Minuten herauszuzögern. Wer sich daran hält, hat wenig zu befürchten.
Komplikationen & Folgen
Wie bei allen Krebserkrankungen, so wartet auch Morbus Hodgkin mit einigen Komplikationen auf. Diese sind jedoch sehr stark vom Stadium der Krankheit abhängig. Bei einem allzu schweren Krankheitsverlauf tritt schließlich auch der Tod als endgültige Komplikation auf.
 Hier eine Übersicht über die gängigsten Symptome:
Hier eine Übersicht über die gängigsten Symptome:
- Geschwächtes Immunsystem
- Unfruchtbarkeit
- Weitere Ausbrüche von Krebs
- Weitere gesundheitliche Probleme
Die genannten möglichen Komplikationen werden nachfolgend noch genauer erläutert. Wie man aus der Liste entnehmen kann, sind die zu erwartenden Komplikationen mit unter sehr gravierend und man sollte einem Arztbesuch darum nicht aus dem Wege gehen, wenn sich Anzeichen darauf einstellen. Nur wer Hilfe sucht, kann sie auch finden.
Alles in allem also, sollte man die Nachsorge sehr ernst nehmen und auch begleitende Angebote nutzen, um nicht nur sehr Risiko auf eine weitere Erkrankung zu reduzieren, sondern auch schlicht, um die Überlebenschancen zu steigern.
Immunschwäche
Geschwächtes Immunsystem
Ein geschwächtes Immunsystem ist eine häufige Komplikation des Hodgkin-Lymphoms und kann während der Behandlung darüber hinaus auch noch schwerer werden.
Wenn man ein schwaches Immunsystem hat, ist man anfälliger für Infektionen und es besteht ein erhöhtes Risiko für die Entwicklung weierer ernsthafter Komplikationen durch Infektionen verschiedenster Arten. In manchen Fällen wird einem möglicherweise geraten, regelmäßig und vorallem prophylaktisch Antibiotika einzunehmen, um Infektionen vorzubeugen.
Es ist auch wichtig, alle Symptome einer Infektion sofort dem Hausarzt oder Pflegeteam zu melden, da eine sofortige Behandlung erforderlich sein kann, um schwerwiegende Komplikationen zu vermeiden. Typische Anzeichen einer solchen Infektion sind unter anderem Kopfweh, Durchfall, Kopfschmerzen, Müdigkeit, Muskelschmerzen, Fieber uvm.
Unfruchtbarkeit
Unfruchtbarkeit ist die Unfähigkeit einer Person, eines Tieres oder einer Pflanze, sich auf natürliche Weise zu vermehren. Normalerweise ist dies nicht der natürliche Zustand eines gesunden Erwachsenen.
Beim Menschen bezeichnet Unfruchtbarkeit die Unfähigkeit, schwanger zu werden, eine Schwangerschaft zu erzeugen oder eine Schwangerschaft bis zum Ende zu auszutragen. Es gibt viele Ursachen für Unfruchtbarkeit, darunter auch einige, die durch medizinische Eingriffe behandelt werden können. Schätzungen deuten darauf hin, dass weltweit etwa fünf Prozent aller heterosexuellen Paare ein ungelöstes Problem mit Unfruchtbarkeit haben.

Eine mögliche Folge ist die Unfruchtbarkeit
Viele Paare erleben jedoch eine mehr oder weniger unfreiwillige Kinderlosigkeit für mindestens ein Jahr, wenn diese damit beginnen, aktiv dem Kinderwunsch nachzugehen. Schätzungen besagen, dass 20 – 30% der Fälle von Unfruchtbarkeit auf männliche Unfruchtbarkeit zurückzuführen sind, 20 – 35% sind auf weibliche Unfruchtbarkeit zurückzuführen und 25-40% sind auf kombinierte Probleme in beiden Teilen zurückzuführen.
In 10-20% der Fälle findet sich keine medzinisch nachvollziehbare Ursache. Die häufigste Ursache für weibliche Unfruchtbarkeit sind ovulatorische Probleme, die sich in der Regel nur spärlich manifestieren und / oder fehlende Menstruationsperioden. Männliche Infertilität ist am häufigsten auf Mängel im Samen zurückzuführen.
Frauen, die fruchtbar sind, erleben eine natürliche Periode der Fruchtbarkeit vor und während des Eisprungs und sie sind für den Rest des Menstruationszyklus natürlich unfruchtbar. Methoden zur Feststellung der Fruchtbarkeit werden verwendet, um festzustellen, wann diese Veränderungen auftreten, indem Veränderungen des Zervixschleims oder der Basaltemperatur verfolgt werden.
Durch den Morbus Hodkin kann die Fruchtbarkeit beider Geschlechter stark vermindert oder sogar komplett ausgelöscht werden. Wer also beispielsweise nach einer erfolgreichen Behandlung einen Kinderwunsch verspürt, sollte sich eventuell mit einem Spezialisten zusammentun, um etwaige Probleme im Vorfeld festzustellen und zu besprechen.
Krebsausbrüche
Weitere Ausbrüche von Krebs
Menschen mit einem Hodgkin Lymphom haben auch in Zukunft, nach einer erfolgreichen Behandlung, häufiger Lymphome, Leukämien oder andere Krebsarten.
Chemotherapie und Strahlentherapie erhöhen dieses Risiko zudem weiter.„Zweitkarzinome“ wie Brustkrebs oder Lungenkrebs entwickeln sich in der Regel mehr als 10 Jahre nach der eigentlichen Behandlung des Hodgkin Lymphoms. In seltenen Fällen entwickeln sich andere Krebsarten wie Leukämie oder andere Lymphome bereits nach wenigen Jahren.
Man kann selbst helfen, das Risiko einer zweiten Krebserkrankung zu reduzieren, indem man einen gesunden Lebensstil pflegt, beispielsweise durch Nichtrauchen, ein gesundes Gewicht durch eine ausgewogene Ernährung halten und sich regelmäßig sportliche betätigen.
Man sollte seinem behandelnden Arzt bereits in einem frühen Stadium alle Symptome melden, die auf einen anderen Krebs hindeuten könnten und an allen Krebsvorsorgeuntersuchungen teilnehmen, die einem empfohlen wurden.
Weitere Probleme
Weitere gesundheitliche Probleme
Das Risiko, in der Zukunft auch noch andere gesundheitliche Probleme, wie etwa Herz-Kreislauf-Erkrankungen und Lungenerkrankungen zu entwickeln, ist bei Menschen mit Morbus Hodgkin ebenfalls höher als bei solchen, die nie an der Krankheit litten.Man sollten seinem Arzt unerwartete Symptome, wie zum Beispiel zunehmende Atemnot, melden, um weitere Ratschläge zu erhalten und auf Nummer sicher zu gehen.
Wann zum Arzt?
Wann sollte man zum Arzt gehen?
Es kann bisweilen recht kompliziert sein, Morbus Hodgkin als solchen zu erkennen. Dies liegt unter anderem daran, dass die Symptome oftmals sehr unspezifisch sind und eine Diagnose somit nicht immer direkt ins Schwarze trifft.
Darüber hinaus sollte man auch nicht vergessen, dass es sich beim Morbus Hodgkin um eine Art von Krebs handelt. Das bedeutet, dass das Leiden sehr schnell sehr gefährlich werden kann und darum auf keinen Fall auf die leichte Schulter zu nehmen ist.
Krebs ist eine nicht selten tödlich verlaufende Erkrankung und sollte darum so schnell als irgend möglich erkannt und behandelt werden. Geschieht dies nicht rechtzeitig, so ist der Verlust des Lebens ein Risiko, mit dem man durchaus rechnen muss.
Darüber hinaus kann es sinnig sein zu überprüfen und nachzuvollziehen, ob man eventuell einer oder gar mehrerer Risikogruppen angehört. Ist dies der Fall, so ist es bisweilen sogar ratsam, sich regelmäßig, auch ohne das auftreten spezifischer Symptome, auf einen eventuellen Ausbruch der Erkrankung hin untersuchen zu lassen.
Diese Thematik sollte man also durchaus gegenüber seinem Hausarzt ansprechen. Vorsicht ist hier besser als Nachsicht und jede Sekunde zählt. Bei Morbus Hodgkin vielleicht sogar noch mehr als bei vielen anderen, weniger aggressiven und gefährlichen Erkrankungen.
Kurzum also sollte man es nicht vernachlässigen, seinem Arzt von seinen eventuellen Sorgen und Problemen zu berichten, wenn man denkt, man könnte Opfer des vorliegenden Leidens geworden sein.
Ein Hausarzt sollte immer ein offenes Ohr für seine Patienten haben. Das stärkt das Vertrauensverhältnis zwischen Arzt und Patienten und trägt darüber hinaus auch dazu bei, dass viele Krankheiten nicht nur früher entdeckt, sondern somit auch gleich besser und effektiver behandelt werden können.
Behandlung & Therapie
Zunächst einmal sei angemerkt, dass es heutzutage glücklicherweise möglich ist, Morbus Hodgkin zu behandeln. Zwar endet noch immer nicht jede Behandlung mit einer vollkommenen Beseitigung des Leidens, aber dennoch kann vielen Patienten nachhaltig geholfen werden.
Insbesondere dann, wenn man die Krankheit früh erkennt und somit auch frühe Hilf erfährt. Als Faustregel kann man sich also merken, dass je früher die Krankheit erkannt wird, desto besser stehen die Chancen auf Heilung.
Der behandelnde Arzt wird die Scans überprüfen und daran Behandlungsoptionen festmachen. Welche Hodgkin Behandlungen am besten geeignet sind, hängt von der Art und dem Stadium der Erkrankung, der allgemeinen Gesundheit und den persönlichen Vorlieben ab.
Das Ziel der Behandlung ist es, so viele Krebszellen wie möglich zu zerstören und die Krankheit somit in die Remission zu zwingen.
Chemotherapie
Eine sehr häufig zur Anwendung kommende Art der Behandlung, ist die Chemotherapie. Bei der Chemotherapie handelt es sich um eine medikamentöse Behandlung, bei der zur Abtötung von Lymphomzellen Chemikalien eingesetzt werden.
Chemotherapie
Chemotherapeutische Wirkstoffe werden in den Blutkreislauf geleitet und können somit fast alle Bereiche des Körpers erreichen. Eine Chemotherapie wird oft mit einer Strahlentherapie bei Menschen mit einem klassischem Hodgkin Lymphom im Frühstadium kombiniert.
Eine Strahlentherapie wird typischerweise nach einer Chemotherapie durchgeführt. Bei einem fortgeschrittenem Hodgkin Lymphom kann die Chemotherapie allein oder in Kombination mit einer Strahlentherapie angewendet werden.
Chemotherapie Medikamente können in Form von Tabletten oder durch eine Vene im Arm des Patienten eingenommen werden. Manchmal werden beide Methoden zeitgleich verwendet. Mehrere Arten von Chemotherapeutika werden zur Behandlung von Morbus Hodgkin eingesetzt. Nebenwirkungen der Chemotherapie hängen von den Medikamenten ab, die man erhält.
Häufige Nebenwirkungen sind Übelkeit und Haarausfall. Schwere Langzeitkomplikationen können darüber hinaus auch auftreten, wie beispielsweise Herzschäden, Lungenschäden, Fruchtbarkeitsprobleme und auch andere Krebsarten wie Leukämie. Letzteres ist allerdings zum Glück eher selten der Fall.
Strahlentherapie
Wie gerade erwähnt, findet auch die Strahlentherapie oftmals Einsatz bei der Behandlung von Morbus Hodgkin. Die Strahlentherapie benutzt energiereiche Strahlen, wie beispielsweise Röntgenstrahlen und Protonen, um Krebszellen abzutöten.
Bei der klassischen Morbus Hodgkin wird häufig eine Strahlentherapie nach Chemotherapie verordnet. Menschen mit nodulärem Lymphozyten prädominantem Hodgkin Lymphom im Frühstadium können oftmals mittels einer Strahlentherapie allein erfolgreich behandelt werden.
Während der Strahlentherapie liegt man auf einem Tisch und eine große Maschine bewegt sich um einen herum und lenkt die dicht gebündelten Energiestrahlen auf bestimmte Punkte des Körpers. Die Bestrahlung kann auf die betroffenen Lymphknoten und den nahe gelegenen Bereich um die Lymphknoten herum gerichtet sein, wo die Krankheit hinausstreuen könnte.
Die Dauer der Strahlenbehandlung variiert je nach Stadium der Erkrankung. Ein typischer Behandlungsplan kann dazu führen, dass man fünf Tage in der Woche für mehrere Wochen ins Krankenhaus oder in die Klinik gehen muss.
Bei jedem Besuch wird man einer etwa 30 minütigen Bestrahlung unterzogen. Eine Strahlentherapie kann Hautrötungen und Haarausfall an der behandelten Stelle verursachen. Viele Menschen leiden darüber hinaus an starker Müdigkeit während der Strahlentherapie. Zu den schwerwiegenderen Risiken zählen Herzerkrankungen, Schlaganfälle, Schilddrüsenprobleme, Unfruchtbarkeit und andere Krebsarten wie Brustkrebs oder Lungenkrebs.
Stammzellentransplantation
Bisweilen kann es auch hilfreich sein, Knochenmark zu therapeutischen Zwecken zu verpflanzen. Eine sogenannte Knochenmarktransplantation, auch bekannt als Stammzellentransplantation, ist eine Behandlung, die das erkrankte Knochenmark durch gesunde Stammzellen ersetzt, die einem dabei helfen sollen, eigenständig neues Knochenmark zu produzieren.
Eine Knochenmarktransplantation kann dann eine Option sein, wenn das Hodgkin Lymphom trotz anderer Arten der Behandlung immer wieder zurückkehrt. Während einer Knochenmarktransplantation werden die eigenen Blutstammzellen entfernt, eingefroren und für die spätere Verwendung gelagert.
Als nächstes erhält man eine hochdosierte Chemobehandlung und Strahlentherapie, um Krebszellen im Körper des Patienten zu zerstören. Schließlich werden die Stammzellen aufgetaut und durch die Venen in den Körper injiziert.
Die Stammzellen helfen einem dabei, gesundes Knochenmark neuerlich aufzubauen. Menschen, die sich einer Knochenmarktransplantation unterziehen, haben möglicherweise ein erhöhtes Infektionsrisiko und dies teilweise auch für den Rest ihres Lebens. Dieses Risiko ist allerdings im Vergleich zu einem Exitus durch Morbus Hodgkin durchaus aushaltbar.
Weitere Methoden
Andere Medikamente, die zur Behandlung von Morbus Hodgkin eingesetzt werden, sind sogenannte „zielgerichtete“ Medikamente, die sich auf spezifische Schwachstellen in den Krebszellen konzentrieren. Auch eine Immuntherapie, die das eigene Immunsystem aktiviert, um die Lymphomzellen abzutöten, ist eine oftmals gewählte Art der Behandlung.
Wenn andere Behandlungen nicht geholfen haben oder wenn das Hodgkin Lymphom nach einer erfolgreich abgeschlossenen Behandlung zurückkehrt, können die Lymphomzellen in einem Labor analysiert werden, um nach genetischen Mutationen zu suchen, die eventuell für die Rückkehr zuständig sind oder um die Medikamente gezielter auswählen zu können.
Der behandelnde Arzt kann einem die Behandlung mit einem bestimmten Medikament empfehlen, das auf bestimmte Mutationen in den eigenen Lymphomzellen abzielt. Gezielte Therapie ist ein aktiver Bereich der Krebsforschung. Neue zielgerichtete Medikamente werden in klinischen Studien immer wieder erfolgreich untersucht.
Fazit
Patienten mit der Erkrankung im Frühstadium können sehr wirksam mit einer Strahlentherapie oder Chemotherapie behandelt werden. Die Wahl der Behandlung hängt von Alter, Geschlecht, der Schwere des Falles und dem histologischem Subtyp der Erkrankung ab.
Die Zugabe einer lokalisierten Strahlentherapie nach der Chemotherapie kann ein längeres progressionsfreies Überleben im Vergleich zur alleinigen Chemotherapie bieten.
Patienten mit einer Erkrankung in einem fortgeschritteneren Stadium werden oftmals nur mit einer Kombinationschemotherapie behandelt. Patienten jeden Stadiums mit größeren betroffenen Arealen im Bereich der Brust werden normalerweise mit kombinierter Chemotherapie und Strahlentherapie behandelt.
Obwohl ein erhöhtes Alter ein ungünstiger Risikofaktor für das Hodgkin Lymphom ist, sind ältere Patienten ohne größere Komorbiditäten im Allgemeinen ausreichend geeignet, um eine Standardtherapie zu tolerieren und erzielen oftmals ein Behandlungsergebnis, das mit dem von jüngeren Patienten vergleichbar ist.
Die Krankheit stellt jedoch bei älteren Patienten eine weitaus größere Gefahr für Leib und Leben dar und darum gehen unterschiedliche Überlegungen in Behandlungsentscheidungen mit ein.
Strahlenonkologen
Bei Morbus Hodgkin benutzen Strahlenonkologen typischerweise eine externe Strahlentherapie. Strahlungsonkologen liefern eine externe Bestrahlung auf das Lymphom mittels einer Maschine, die auch als Linearbeschleuniger bekannt ist. Hierin werden hochenergetische Röntgenstrahlen und Elektronen erzeugt.

Strahlentherapie
Patienten beschreiben Behandlungen in der Regel als schmerzlos und vom Gefühl her ähnlich wie eine Röntgenaufnahme. Die Behandlungen dauern im Schnitt weniger als 30 Minuten.
Bei Lymphomen gibt es verschiedene Wege, wie Strahlentherapeuten genau auf die zu behandelnden Krebszellen zielen können. Die involvierte Strahlung ist, wenn die Strahlungsonkologen Strahlung nur an jene Teile des Körpers des Patienten abgeben, von denen bekannt ist, dass sie Krebs haben, am effektivsten.
Sehr oft ist dies mit einer Chemotherapie kombiniert. Eine Strahlentherapie, die über das Zwerchfell zu Hals, Brust oder Achselhöhlen gerichtet ist, wird bisweilen auch als Mantelfeldstrahlungstherapie bezeichnet.
Strahlung unterhalb des Zwerchfells zu Bauch, Milz oder Becken wird als invertierte Y-Feldstrahlung bezeichnet. Die gesamte Lymphknotenbestrahlung erfolgt, wenn der Therapeut alle Lymphknoten im Körper mit Strahlung beschießt, um Zellen zu zerstören, die sich möglicherweise ausgebreitet haben.
Vorbeugung & Prävention
Leider, so muss man sagen, ist es kaum möglich, dem Morbus Hodgkin in irgendeiner Form vorzubeugen. Es gibt keine in der Schulmedizin anerkannten Methoden, die dazu imstande wären, die vorliegende Erkrankung herauszuzögern oder komplett daran zu hindern, dass sie entsteht.
Daher finden sich leider auch keine Impfstoffe oder andere präventiv zu reichende Medikamente auf dem Markt. Wer derartiges postuliert und versucht auf diese Art und Weise Produkte zu verkaufen, kann nur als Scharlatan gelten und sollte tunlichst gemieden und am besten auch angezeigt werden.
Risiken mindern
Nichtsdestotrotz gibt es einige Mittel und Wege, derer man sich bedienen kann, um zumindest die gröbsten Risikofaktoren etwas zu minimieren. Gleichwohl auch hier an dieser Stelle noch einmal gesagt werden sollte, dass einige dieser Faktoren, allen voran das Alter, unausweichlich sind. Schließlich und endlich kann man den Prozess des Alterns (noch) nicht aufhalten und somit auch die Chancen auf eine Entstehung von Morbus Hodgkin nicht wirklich senken.
Was natürlich immer gut und empfehlenswert ist, ist eine allgemein gesunde und körperbewusste Lebensführung. Wer nicht raucht, keinen Alkohol konsumiert, sich gesund ernährt, Sport treibt und sich viel in der Natur aufhält, ist zwar nicht automatisch gegen die vorliegende Erkrankung gefeit, dennoch senkt sich das Risiko eines Ausbruchs generell etwas ab.
Darüber hinaus senkt sich auch das Risiko der Entstehung anderer Erkrankungen auf diese Art und Weise ab. Nicht zuletzt darum sollte man verstärkt darauf achten, keinen Raubbau an seinem eigenen Körper zu betreiben, sondern gesund und ausgewogen zu leben.
Eine andere Art der „Prävention“ ist es, regelmäßig bei einem Mediziner vorstellig zu werden und sich auf den eventuellen Ausbruch von Morbus Hodgkin testen zu lassen. Wer dies tut. Ist zumindest auf der sicheren Seite, wenn es darum geht, eine möglist frühe Erkennung des Leidens zu gewährleisten.
Alles in allem also lässt sich leider nur konstatieren, dass es keine richtigen Maßnahmen zur Vorbeugung gibt, die die Entstehung des Morbus Hodgkin zu großen Teilen ausschließen würden. Dennoch gibt es einige Sicherheitsmaßnehmen, die man treffen kann, um zumindest das Risiko des Ausbruchs etwas zu minimieren.
Prognose zur Heilung
Die Behandlung von Morbus Hodgkin hat sich in den letzten Jahrzehnten glücklicherweise stark verbessert. Jüngste Studien, bei denen neuere Arten von Chemotherapie untersucht wurden, konnten höhere Überlebensraten als zuvor anzeigen.
In einer kürzlich durchgeführten europäischen Studie lag die 5 Jahres Überlebensrate bei Patienten mit einer günstigen Prognose bei stolzen 98%, bei Patienten mit schlechteren Aussichten bei mindestens immerhin noch 85%.
Im Jahr 1998 identifizierte eine internationale Studie sieben prognostische Faktoren, die die Erfolgsrate der konventionellen Behandlung bei Patienten mit lokal ausgedehntem oder fortgeschrittenem Hodgkin Lymphom genau vorhersagen.
Das Ausbleiben eines Rückfalls nach 5 Jahren stand in direktem Zusammenhang mit der Anzahl der bei einem Patienten vorhandenen vorher festgelegten Faktoren. Der 5 Jahres Überlebensfaktor für Patienten mit Nullfaktoren beträgt rund 80%.
Die eben erwähnten negativen prognostischen Faktoren, die in der internationalen Studie identifiziert wurden, sind:
- Das Alter
- Das Stadium der Krankheit zum Zeitpunkt der ersten Behandlung
- Der Hämoglobinwert
- Die Anzahl der Lymphozyten
- Das Geschlecht (besonders Männer sind rückfallgefährdet)
- Die Anzahl weißer Blutkörper
- Lebensführung
Weitere Studien
Weitere Studien berichteten über die folgenden ungünstigen prognostischen Faktoren: gemischte zelluläre oder lymphozytendepletierte Histologien, männliches Geschlecht, große Anzahl von involvierten Lymphknoten, fortgeschrittenes Stadium der Erkrankung zum Zeitpunkte der Diagnose, Alter von 40 Jahren oder mehr, das Vorhandensein von weiteren Symptomen (Fieber, Nachtschweiß etc) und eine hohe Erythrozytensedimentationsrate.
Darüber hinaus können auch krankhafte Vergrößerungen der Lymphknoten ein klarer Indikator dafür sein, dass ein Patient zu einem Rückfall neigt.
In jüngerer Zeit hat die Positronen-Emissions-Tomographie (PET) früh nach Beginn der Chemotherapie eine stark positive prognostische Wirkung gezeigt. Dies ermöglicht eine Beurteilung der Reaktion eines Individuums auf eine Chemotherapie, da die PET-Aktivität bei ansprechenden Patienten schnell abklingt.
In einer Studie nach zwei Zyklen einer Chemotherapie waren 83% der Patienten nach 3 Jahren immer noch krankheitsfrei, wenn sie darüber hinaus auch ein negatives PET Ergebnis hatten. Dem gegenüber nur 28% bei Patienten mit positiven PET-Scans. Diese prognostische Aussagekraft übertrifft herkömmliche oben diskutierte Faktoren.
Mehrere Studien sind derzeit im Gange, um zu sehen, ob eine PET-basierte risikoadaptierte Reaktion verwendet werden könnte und sollte, um die Patientenergebnisse zu verbessern, indem die Chemotherapie früh bei Patienten, die nicht ansprechen, gegen einen anderen therapeutischen Ansatz getauscht wird.
Kurzum ist die Prognose von Fall zu Fall sehr unterschiedlich und man sollte keine voreiligen Schlüsse ziehen. Es besteht beinahe immer Hoffnung, dennoch aber sollte man sich auch mit dem Gedanken anfreunden, dass die Krankheit keinen positiven Verlauf nehmen könnte. Eine psychologische Beratung könnte in diesem angebracht sein.
Hodgkin Subtypen
Die verschiedenen Formen von Hodgkin
Die Weltgesundheitsorganisation (WHO) klassifiziert Morbus Hodgkin in fünf Subtypen – 4 werden als klassisches Morbus Hodgkin bezeichnet und eine wird getrennt als „Nodulär sklerosierende Form“ klassifiziert.
Diese Klassifikationen basieren darauf, wie die Lymphomzellen unter einem Mikroskop aussehen. Dies umfasst die Art der Lymphomzellen, wie sie organisiert sind und noch andere Merkmale, die in der Probe aus dem Lymphknoten zu sehen sind.
Die verschiedenen Arten von Morbus Hodgkin können in den Lymphknoten in verschiedensten Teilen des Körpers beginnen und betroffen darüber hinaus Menschen in unterschiedlichem Alter, wie bereits eingänglich erwähnt. Einige Arten sind häufiger Verursacher spezifischer Symptome, wie beispielsweise Fieber von 38 ° C oder höher, nächtliches Schwitzen und ungeklärten Gewichtsverlust von mehr als 10% des Körpergewichts binnen kürzester Zeit.
- Nodulär sklerosierende Form
- Gemischtzellige Form
- Lympozytenreiche Form
- Lympozytenarme Form
- Nodular lymphozytenprädominante Form
Wie aus dieser Liste hervorgeht, ist Morbus Hodgkin nicht gleich Morbus Hodgkin. Das macht eine Diagnose nicht immer ganz einfach und es ist bisweilen notwendig, mehrere Tests durchzuführen, um die genaue Art der vorliegenden Erkrankung zu ermitteln, um schließlich dazu in der Lage zu sein, den optimalen therapeutischen Ansatz zu finden.
Nodulär sklerosierend
Nodulär sklerosierende Form
Die nodulär sklerosierende Form ist die häufigste Art von Morbus Hodgkin. Sie macht zwischen 60 – 80% aller Fälle aus. Sie tritt gleichermaßen häufig bei Männern und Frauen auf. Der er nodulär-sklerosierende Typ entwickelt sich normalerweise bei Teenagern und jungen Erwachsenen zwischen 15 und 35 Jahren.
Die hierdurch entstehenden Symptome sind zumeist nicht allzu gravierend, auch dann nicht, wenn das Leiden bereits eine Gefahr für Leib und Leben darstellt. Darum zeigt sich auch hier wieder, dass man bereits kleinste Symptome als Anlass für eine Behandlung nehmen sollte.
Gemischtzellig
Gemischtzellige Form
Gemischte Zellularität ist die zweithäufigste Art von Morbus Hodkin. Sie macht zwischen 15 – 30% aller Fälle aus. Sie wird am häufigsten bei älteren Erwachsenen beobachtet und ist die Art von Morbus Hodkin, die am häufigsten bei Menschen mit hiv-Infektion beobachtet wird.
Die vorliegende Form der Erkrankung kann in jedem Lymphknoten beginnen. Sie entwickelt sich meist in der oberen Körperhälfte und befällt in der Regel Lymphknoten im Bauchraum und in der Milz. Das Leiden ist oftmals schon weiter fortgeschritten, wenn es diagnostiziert wird und normalerweise mit deutlich wahrnehmbaren Symptome verbunden.
Lymphozytenreich
Lympozytenreiche Form
Der lymphozytenreiche Form des Morbus Hodgkin macht etwa 5% aller Fälle aus. Die Krankheit ist häufiger bei älteren Menschen anzutreffen und entwickelt sich ebenfalls häufiger bei Männern als bei Frauen.
Darüber hinaus entwickelt sie sich normalerweise in den Lymphknoten des Nacken, der Achselhöhlen und oberhalb des Schlüsselbeins. Sie wird meist in einem frühen Stadium (Stadium 1 oder 2) diagnostiziert und betrifft selten mehr als einige wenige Lymphknoten.
Symptome bleiben entweder ganz aus oder sind nur sehr geringfügiger Natur. Das allerdings macht die Krankheit als solche auf keinen Fall weniger gefährlich oder lebensbedrohlich.
Lymphozytenarm
Lympozytenarme Form
Die lympozytenarme Variante ist die am wenigsten häufige Art von Morbus Hodgkin. Sie macht nur etwa 1% aller Fälle aus. Sie ist zudem häufiger bei älteren Menschen anzutreffen und entwickelt sich darüber hinaus häufiger bei Vertretern des männlichen Geschlechts als bei Frauen. Menschen mit aids oder hiv sind außerdem vergleichsweise häufiger betroffen als nicht daran leidende Individuen.
LPHD
Nodular lymphozytenprädominante Form (LPHD)
Diese Form der vorliegenden Erkrankung macht etwa 5% aller Fälle aus. Diese Art von Morbus Hodgkin bedingt die Entstehung abnormaler Zellen, die auch LP-Zellen genannt werden. Bisweilen werden sie wegen ihres Aussehens unter dem Mikroskop auch als Popcorn-Zellen bezeichnet (diese Zellen wurden früher lymphozytäre und histiozytäre Zellen genannt).
Es können sehr wenige oder keine Hodgkin-Zellen in der Probe aus dem Lymphknoten vorhanden sein, was die Diagnose ungleich erschweren kann. Diese Form des Lymphoms kann in jedem Alter auftreten, aber es ist am häufigsten bei jungen Männern zu beobachten.
Es beginnt in der Regel mit einem Befall der Lymphknoten im Nacken und in der Achselhöhle. Es ist in der Regel langsam wachsend oder indolent und in einem frühen Stadium ohne große Probleme erkennbar und diagnostizierbar.
Die meisten Menschen weisen keine anderen Symptome als vergrößerte Lymphknoten im Nacken, in den Achselhöhlen oder der Leistengegend auf. Andere Symptome sind sehr selten.
Alternative Medizin
Es gibt einige alternative Therapieansätze, die dabei helfen können, gegen Morbus Hodgkin vorzugehen. Dennoch sollte man eine schulmedizinische Behandlung nicht vernachlässigen!
Wer dies tut, muss damit rechnen, dem Leiden schließlich zu erliegen. Die Kombination aus alternativen und schulmedizinischen Methoden ist hier wohl die beste.
 Hierzu eine Übersicht:
Hierzu eine Übersicht:
- Infusionstherapie
- Vitamin C Therapie
- Gerson Therapie
Bevor man sich jedoch endgültig für eine solche alternative Therapie entscheidet, sollte man auf jeden Fall Rücksprache mit seinem behandelnden Arzt halten! Alleingänge können hier tödlich enden. Das sollte man niemals vergessen.
Infusionstherapie
Infusionstherapien sind allgemeine Regenerationstherapien, die unter anderem Vitamin C und B17 verwenden. Der Unterschied zwischen Injektionen und oraler Medikation liegt in der Tatsache, dass das Personal gut ausgebildet sein muss, um die Injektionsnadel an die richtige Stelle zu setzen. Dies erfordert gut ausgebildete Menschen und eine Organisation, die es ihren Mitarbeitern ermöglicht, sich die Zeit zu nehmen, die nötig ist, um die Dinge richtig und entsprechend den Bedürfnissen der Patienten zu erledigen.
Amygdalin-B17 beispielsweise wird bei Infusionstherapien und in natürlichen Chemotherapien verwendet. Amygdalin, Laetrile oder B17 ist eine natürliche Substanz, die unter anderem in Aprikosenkernen gefunden werden kann, aber B17 ist auch in den Kernen von Pfirsichen, Nektarinen, Kirschen, Pflaumen oder Äpfel enthalten und ist auch in Buchweizen, Brokkoli, Spinat, Blumenkohl oder Cashewnüssen zu finden.
Aus chemischer Sicht besteht B17 aus einem Molekül Benzaldehyd (ein Schmerzmittel) und einem Molekül Cyanwasserstoff (Cyanwasserstoffsäure). Gesunde Zellen sind von diesem Prozess nicht betroffen, da sie ein Enzym namens Rhodanese enthalten. Das Rhodanase-Enzym kann Cyanwasserstoffsäure (in B17 vorhanden) in Thiocyanat umwandeln.
Thiocyanat wirkt sich positiv auf den Organismus aus, da Thiocyanat den Blutdruck senkt und weiterhin auch eine Substanz ist, mit der der Organismus den zur Nervenernährung notwendigen Stoff b12 herstellt. Benzaldehyd (in B17 enthalten) wird in gesunden Zellen mit Hilfe von Sauerstoff in das natürliche Schmerzmittel Benzoesäure umgewandelt.
Die Eigenschaften von B17 lassen darauf schließen, dass B17 als Nahrung für gesunde Zellen und als Gift für Krebszellen angesehen werden kann. Da die Therapie zur natürlichen Regulierung unseres Stoffwechsels eingesetzt wird, kann sie als 2natürliche Chemotherapie“ angesehen werden.
Vitamin C Therapie
C ist ein essentieller Mikronährstoff, ohne den wir kein gesundes Leben führen können. Hochdosierte Vitamin C-Infusionen sind Teil einiger alternativer Regulationstherapien.
Vitamin C gehört zur wasserlöslichen Klasse von Vitaminen. Es kann nicht vom Körper selbst produziert werden, noch kann es im Körper gespeichert werden. Es ist schnell verbraucht und überschüssiges Material wird ausgeschieden.
Der Mensch ist daher täglich darauf angewiesen, Vitamin C in seiner Nahrung zu sich zu nehmen. Vor allem Krebspatienten leiden oft an einem Mangel an Vitamin C aufgrund von Chemotherapie, Appetitlosigkeit oder erhöhtem Energieverbrauch. Eine künstliche Ergänzung dieses Vitamins wirkt daher manchmal wahre Wunder
Gerson Therapie
Die Gerson Therapie, entwickelt von dem deutschen Arzt Dr. Max Gerson, ist die am längsten bestehende und am meisten anerkannte Behandlung, die die Selbstheilungskräfte des Körpers aktivieren soll.
Die Gerson Diät schlägt dabei eine biologische und vegetarische Diät einschließlich roher Säfte, Kaffeeeinläufe und natürlicher Ergänzungen in Form diverser Präperate vor. Die Patienten folgen einem sehr detaillierten Therapieplan mit der täglichen Einnahme von Nahrungsergänzungsmitteln.
Man integriert die Therapie oftmals mit anderen ganzheitlichen Ansätzen. Entweder kann sie als integrative Krebstherapie oder als eigenständige Regenerationstherapie zum Einsatz kommen.
Patienten, die sich für diese Art der Behandlung entscheiden, erhalten in den Spezialkliniken oftmals ein breites Spektrum an integrativen Krebstherapien, wie Regulation, Regeneration und dergleichen.
Um all diese Therapien unter einen Hut zu bekommen, wenden viele Kliniken modifizierte Formen der Gerson Therapie an. Spezielle Rezepte sind ein einfacher Weg, um mit der Therapie zu beginnen und nicht zu viel Vorbereitung auf sich nehmen zu müssen.
Smoothie Rezepte dienen als Anleitung für den Einstieg in diese Therapie. Sie sind morgens leicht zubereitet und halten den ganzen Tag vor. Man kann sie verwenden, wenn man zu Hause ist oder wenn man unterwegs ist.
Mit der Zugabe einer modifizierten Gerson Therapie zu den täglichen Therapieplänen können Patienten ihre Ernährungstherapien fortsetzen und gleichzeitig moderne biologische Krebstherapien erhalten.
Dieser Ansatz ist besonders bei Blocktherapien interessant, da Patienten während des Aufenthalts in einer Spezialklinik lernen, eine modifizierte Form der Therapie auch selbstständig im Alltag anzuwenden, sobald sie wieder zu Hause und somit auf sich gestellt sind.
Zumeist werden die Patienten durch eine organische und vegetarische Ernährung mit Rohsäften, Kaffeeeinläufen und natürlichen Ergänzungsmitteln aktiv in diese regulierende Krebstherapie eingebunden.
Patienten, die sich einer regulativen Krebstherapie mittels der Gerson Diät unterziehen, erhalten neben ihren regulativen Krebstherapiemodulen oftmals auch Anleitungen, die gesamten Therapiesitzungen besser verständlich und die Notwendigkeit mancher Schritte sichtbar machen.
Hodgkin Hausmittel
Hilfreiche Hausmittel bei Morbus Hodgkin
Zwar gibt es einige Hausmittel, die sich förderlich auf die Heilung von Morbus-Hodgkin auswirken, man sollte diese aber nur unterstützend zu einer schulmedizinischen Therapie anwenden. Nicht etwa als ein kompletter Ersatz dafür.

Viel Omgea-3 ist bswp. in fetten Fischen wie Lachs enthalten
Einige der effektivsten Hausmittel für Lymphome bestehen in der Verwendung von
- Jod
- Grüntee-Extrakt
- Artemisinin
- Petersilie
- Süßholz
- Mariendistel
- Reishi Pilze
- Sonneneinstrahlung
- Omega-3-Fettsäuren
- Olivenblatt-Extrakt
- Probiotika
Sowie einer Verringerung von:
Wie bei allen anderen Krebsarten gibt es keine formale Heilung, aber es gibt anerkannte Behandlungsstrategien, die Krebs in Remission versetzen und die Lebensqualität verbessern können, einschließlich Operationen, Chemotherapien, Immuntherapien und gezielten medikamentösen Therapien.
Allerdings gibt es einige intensive Nebenwirkungen für diese verschriebenen Behandlungen, um die Nebenwirkungen dieser Behandlungen zu verringern und um die starken Medikamente gegen Krebs, die oft verschrieben werden, zu ergänzen, werden häufig Hausmittel eingesetzt.
Heilmittel
Die Symptome von Morbus Hodgkin umfassen, wie bereits mehrfach erwähnt, vergrößerte oder verhärtete Lymphknoten, Nachtschweiß, Fieber, Gewichtsverlust, Müdigkeit, Juckreiz und Atemnot.
Hierzu eine Übersicht:
- Sonnenschein: Vitamin D aus der Sonne ist wohl das einfachste Hausmittel gegen Lymphome, da man nur hinausgehen muss, um die dadurch entstehenden Vorteile zu genießen. Vitamin D beseitigt aktiv viele der Symptome von Hodgkin. Obwohl es nicht immer einfach ist, kann eine gesunde Dosis Sonnenschein den Krebs in Schach halten.
- Omega 3 Fettsäuren: Wie immer gehört sogenanntes „gutes“ Cholesterin auf jede Hausmittelliste. Sie stärken das Immunsystem und helfen dem Patienten dabei, schneller zu genesen und mit den Strapazen einer Chemotherapie besser fertig zu werden.
- Mit dem Rauchen aufhören: Rauchen löst nicht nur Lungenkrebs aus. Auch andere Formen von Krebs lassen sich direkt mit diesem Laster in Verbindung bringen. Ob Morbus Hodgkin dazugehört ist zwar diskutabel, dennoch sollte man, erhält man die entsprechende Diagnose, sofort mit dieser Angewohnheit brechen, um schlimmeres zu vermeiden. Dasselbe gilt im übrigen auch für den Konsum von Alkohol.
Heilkräuter & Heilpflanzen
- Petersilie
- Süßholzrinde
- Quecke
- Digitalis Purpurea
- Huflattich
- Diverse Kakteenarten
- Äpfel und Apfelblüten
können mitunter verblüffende Effekte liefern und massiv zur Heilung eines erkrankten Individuums beitragen. Das steht außer Frage. Dennoch sollte man sich, gerade im Falle allzu gravierender Erkrankungen, wie beispielsweise Krebs, nicht ausschließlich auf diese verlassen, sondern auch eine schulmedizinische Behandlung in Anspruch nehmen.
Ansonsten sind die oben genannten Kräuter und anderen Pflanzenbestandteile entweder roh oder Form von Tees oder Pulvern zu genießen. Einige können auch Gewürze verwendet werden. Manche dieser Pflanzen finden sich sehr leicht, beispielsweise im Einzelhandel, andere können über das Internet oder im Fachhandel bezogen werden. Vor der Verwendung, sollte man sich jedoch immer von der Qualität und der Authentizität der erworbenen Kräuter und Pflanzen überzeugen, um ein böses Erwachen zu vermeiden.
Es empfiehlt sich zudem, vor der Anwendung Rücksprache mit dem zuständigen Mediziner zu halten um etwaige allergische Reaktion schon im Vorfeld ausschließen zu können.
Ätherische Öle
- Mandarine
- Orange
- Zimtrinde
- Kirsche
- Ackerminze
- Nelke
- Weihrauch
Die meisten ätherischen Öle dienen lediglich einer Anwendung in Form einer sogenannten Aromatherapie. Eine äußere oder gar innere Anwendung ist in vielen Fällen weniger empfehlenswert oder sollte komplett vermeiden werden, da sie etwaige gravierende Komplikationen nach sich ziehen kann. Eine Aromatherapie hingegen ist oftmals sehr beruhigend für das erkrankte Individuum und hilft darüber hinaus, das Leid etwas zu verringern und dem gestressten Leidenden etwas Ruhe zu verschaffen.
Um eine Aromatherapie durchführen zu können, bedarf es lediglich der entsprechenden Öle, einer Duftlampe, einer Wärmequelle, zumeist einer Kerze und etwas Wasser. Immer mehr kommen auch sogenannte Aromadiffuser in Mode. Diese dienen allerdings besser dazu, einen guten Geruch in der Wohnung zu verbreiten. Für eine wirksame Aromatherapie ist die gute alte Öllampe immer noch das am besten geeignetste Instrument.
Eine gute Bezugsquelle für ätherische Öle ist das Internet oder der Heilpraktiker des Vertrauens. Letzterer gibt auch Auskünfte über Anwendung und Dosierung.
Homöopathie & Globuli
- Apis mellifica
- Nux vomica
- Causticum Hahnemanni
- Belladonna
- Petroselinum
ist heutzutage auch aufgrund der medizinischen Forschung gut erfasst und auch in Bezug auf ihre Wirksamkeit hin überprüft. Dabei hat sich gezeigt, dass in der Mehrzahl der Fälle durch Globuli und Co. keine Wirkung erzielt werden konnte. Der Grund hierfür ist wohl vorallem die Rezeptur der angewandten Mittel und Wirkstoffe.
Um es einmal geradeheraus auszudrücken: Bei Globuli handelt es sich zumeist um nicht viel mehr als kleine Zuckerperlen, die mit immens geringen Dosen der angegeben Wirkstoffe versetzt worden sind. Diese Dosen sind teilweise so gering, dass sie selbst in Laboruntersuchungen nicht mehr nachgewiesen werden können. Mischverhältnisse von 1 zu 10.000.000.000 sind hierbei keine Seltenheit.
Menschen, die jedoch auf Homöopathie schwören, dürften wohl in erster Linie von einem positiven psychosomatischen Effekt profitieren und weniger durch die tatsächlich enthaltenen Wirkstoffe geheilt werden. Nicht zuletzt darum, sollte eine Behandlung mit homöopathischen Mitteln, eine Behandlung schulmedizinischen Medikamenten niemals ersetzen, sondern höchstens begleiten.
Die genauen Dosierungen für die oben genannten Präparate sind stark vom vorliegenden Fall abhängig. Im Groben kann man aber von folgender Dosierung ausgehen:
Oder man entnehme die genauen Dosierungshinweise der Packungsbeilage oder halte Rücksprache mit dem zuständigen Heilpraktiker.
Schüssler-Salze
Hilfreiche sind die Schüssler-Salze Nr.:
- 17 Manganum sulfuricum: Hierbei handelt es sich um einen Wirkstoff, der der Beförderung der Nerven und der Belastbarkeit gilt. Da gerade das Nervenkostüm im Falle starker Krankheiten besonders überlastet ist, kann die Gabe dieses Wirkstoffes auf keinen Fall schaden.
- 7. Magnesium Phosphoricum: Dieses Mittel ist ein richtiger Alleskönner. Es entspannt den Organismus und den Leib und verleiht ihm zudem auch noch Stärke. Hieraus resultiert, dass das betreffene Gebrechen weniger stark auf den Körper einwirkt und zumeist auch schwächer.
- 8 Natrium chloratum: Bei diesem Schüssler Salz handelt es sich um eines, das dabei hilft, die Versorgung des Körpers mit Nährstoffen zu regulieren. Das ist gerade bei Krebserkrankungen sehr wichtig. Darum sollte dieses Schüssler Salz niemals fehlen.
- 18 Calcium sulfuricum Hahnemanni: Dieses Mittel kombiniert ein zum einen Körpergifte bindende als auch anti-inflammatorische Wirkungsspektrum. Darum ist es vornehmlich im Falle von Morbus Hodgkin besonders empfehlenswert.
können die Heilung einiger Krankheiten positiv unterstützen. Zumindest empfinden diese viele Anwender so. medizinisch nachweisen lässt sich diese Wirkung allerdings nicht. Darum sollte man sie lediglich unterstützend, nicht aber ausschließlich anwenden, wenn es um die Behandlung von Krankheiten geht. Insbesondere dann nicht, wenn die Situation so gravierend und ernst ist, wie bei Morbus Hodgkin.
Diät & Ernährung
Die Ernährung spielt in Bezug auf Morbus Hodgkin nur eine unbedeutende Rolle. Diese Art von Krebs wird vermutlich eher weniger, wenn überhaupt durch bestimmte Lebensmittel beeinflusst oder befördert. Allein im Rahmen der vorbeugenden Möglichkeiten, empfehlen einige Mediziner, besonders hohe Mengen an Vitamin C, Omega 3 Fettsäuren und Vitamin B12 zu sich zu nehmen, da sich diese positiv auf das lymphatische System auswirken können.
 Außerdem empfehlen Fachleute, tendenziell eher auf rotes und auf sehr fettes Fleisch wenn es geht zu verzichten.
Außerdem empfehlen Fachleute, tendenziell eher auf rotes und auf sehr fettes Fleisch wenn es geht zu verzichten.
Alles in allem ist eine gesunde Ernährung sehr vorteilhaft und hilft dem Organismus dabei, die Behandlung besser zu überstehen und auch allgemein besser mit dem Leiden fertig zu werden. Man sollte jedoch, bevor man sich für eine spezielle Art der Ernährung entscheidet, Rücksprache mit seinem behandelnden Arzt halten, ob diese auch sinnvoll ist.
Denn gerade während der Chemotherapie, essen viele Menschen schlichtweg nicht genug. Diese zu wenig aufgenommen Kalorien, müssen irgendwie und irgendwo aufgefangen werden, damit der Körper über genügend Reserven verfügt, um die Krankheit und die Therapie überstehen zu können.
Wer sich jedoch sehr unsicher ist, dem ist gerade, einen Ernährungsberater aufzusuchen und einen individuellen Ernährungsplan zu entwickeln. Hiermit macht man nie etwas falsch und es kann sehr gut helfen.
FAQ – Fragen & Antworten
Hier finden Sie Antworten auf häufig gestellte Fragen zu Morbus Hodgkin.
Lymphatisches System?
Was ist das lymphatische System?
Das lymphatische System hilft dem Körper dabei, Krankheiten und andere Gebrechen zu bekämpfen. Das lymphatische System besteht aus einer Reihe von dünnen Röhren und Gruppen von Lymphknoten, die im ganzen Körper anzutreffen sind. Diese Schläuche tragen eine Flüssigkeit, genannt Lymphe, in sich, durch die die Lymphknoten versorgt werden. Diese farblose und wässrige Flüssigkeit ist reich an weißen Blutkörperchen.
Lymphozyten sind der Haupttyp der vorhnadnene Zellen. Sie helfen dem Körper dabei, Infektionen abzuwehren. Ein Lymphknoten hat ungefähr die Größe einer Erbse und weist eine große Anzahl von Lymphozyten auf.
Gruppen von Lymphknoten finden sich im Magen, in der Brust, in der Leistengegend und im Nacken. Einige der inneren Organe des Körpers sind auch Teil des Lymphsystems. Diese Organe umfassen unter anderem das Knochenmark, die Milz, den Thymus und die Mandeln. Andere Organe, wie Teile des Verdauungstrakts, enthalten auch Lymphgewebe. Lymphome können überall dort beginnen, wo Lymphgewebe vorhanden ist.
Hodgkin Behandlung?
Wie sieht eine Behandlung aus?
Es gibt viele verschiedene Arten von Hodgkin Lymphomen. Die Behandlung jedes Lymphoms hängt von der Art des Lymphoms selbst und von dem Stadium ab, also davon, wie weit sich der Krebs bereits ausgebreitet hat. Manche Menschen mit langsam wachsenden Lymphomen müssen möglicherweise nicht sofort behandelt werden.
In einem sehr frühen Stadium kann Strahlung die Hauptbehandlung darstellen. Eine Kombination aus Chemotherapie und Medikamenten ist die häufigste Art der Behandlung.
Es stehen viele verschiedene Therapien zur Verfügung. Es gibt auch eine Immuntherapie, die Medikamente verwendet, um das körpereigene Immunsystem bei der Bekämpfung des Lymphoms zu unterstützen.
Und es gibt Medikamente, die zwecks einer gezielten Therapie eingesetzt werden können. Diese greift nur bestimmte Teile von Lymphomzellen an. Oft werden mehrere Arten von Behandlungen zusammen verwendet. In Fällen, in denen die Behandlung nicht mehr funktioniert, kann der zuständige Medziner eine hochdosierte Chemotherapie und eine Stammzelltransplantation vorschlagen. Dies wird auch als Knochenmarkstransplantation bezeichnet.
Auslöser & Vermutungen?
Wodurch wird Morbus Hodgkin ausgelöst?
Experten wissen nicht, was diese Krankheit verursacht. Viele mögliche Ursachen wurden aber bereits untersucht und es es laufen immer noch viele Studien, die diesem Rätsel auf den Grund gehen sollen.
Zu den stärksten Vermutungen gehören Viren und diverse Umweltfaktoren. Beispielsweise auch das Epstein Barr Virus und das hiv-Virus scheinen beide an der Entstehung einiger Hodgkin Arten beteiligt zu sein. Aber es ist nicht klar, wieso Hodgkin häufiger bei Männern, bei Menschen bestimmten Alters und bei Menschen mit einer familiären Vorbelastung mit der Krankheit auftritt.